Organozirkoniumchemie

De organozirkoniumchemie bestudeert die verbindingen waarin een directe binding tussen koolstof en het metaal zirkonium voorkomt. De organozirkoniumchemie is daarmee een subdiscipline van de organometaalchemie.[1] In het algemeen zijn organozirkoniumverbindingen stabiel en niet toxisch. In de synthetische organische chemie worden de verbindingen toegepast als tussenstap in grotere syntheses. Daarnaast functioneren ze in de vorm van Kaminsky-katalysatoren in de productie van polymeren met speciale eigenschappen. Een aantal eigenschappen delen de organozirkoniumverbindingen met de organotitaniumverbindingen en organohafniumverbindingen, wat niet vreemd is omdat ook deze metalen zich in dezelfde groep van het periodiek systeem bevinden.
De eerste organozirkoniumverbinding die in 1953 beschreven werd was een lid van de metalloceenfamilie: zirkonoceendibromide.[2] De verbinding kon bereid worden in een reactie tussen cyclopentadienylmagnesiumbromide en zirkonium(IV)chloride. Zirkonocenen worden toegepast als polymerisatiekatalysatoren, zoals de eerder genoemde Kaminsky-katalysator. In deze toepassing worden de organotitaniumverbindingen deels verdrongen.
Hydrozirkonering
Schwartz' reagens (1974) is een zirkonoceenhydrochloride dat wordt toegepast in hydrometallatiereacties, die in dit geval hydrozirkonering genoemd worden. In de synthetisch-organische chemie wordt dit type reagens veel toegepast.
Als reactiepartners in de hydrozirkonering treden alkenen en alkynen op. Met eindstandige alkynen wordt voornamelijk het eindstandige zirkoniumproduct gevormd. Daarnaast treden nucleofiele addities, transmetallaties,[3] nucleofiele geconjugeerde addities,[4] koppelingsreacties, carbonyleringen en halogeneringen op.
Geschiedenis
De ontwikkeling van de organozirkoniumhydriden ging vooraf aan het gebruik van deze verbindingen in de hydrozirkonering. Het eerste hydride van dit type, Cp2ZrH2, werd in 1966 ontwikkeld door M.G.H. Wallbridge door reactie van (Cp)2Zr(BH4)2 met tri-ethylamine in benzeen. Het bleek uiteindelijk een tamelijk teleurstellende onoplosbare vaste stof te zijn.[5] In 1970 konden H. Weigold en P.C. Wailes op basis van het dichloride en lithiumaluminiumhydride (of het nauw verwante LiAlH(t-BuO)3) het hydrochloride bereiden: (Cp2ZrClH).[6] De reacties van de nieuwe hydriden met carbonzuren vormden een eerste studieobject[7] (waarbij verbindingen als CpZr(OCOR)3 werden gevormd), in 1971 werden de reacties met alkynen onder de loep genomen.[8]
Zo wordt bij de reactie van één equivalent Cp2ZrClH met difenylacetyleen de overeenkomstige alkenylzirkoniumverbinding als een mengsel van cis- en trans-isomeren gevormd. Met twee equivalenten was het reactiepoduct een mengsel van erythro- en threo-zirkoniumalkanen:

In 1974 pasten Donald W. Hart en Jeffrey Schwartz de verbindingen in de organische synthese toe door de organozirkoniumverbindingen met elektrofielen als zoutzuur, dibroom en zuurchlorides te laten reageren, waarbij de overeenkomstige alkanen, broomalkanen en ketonen ontstonden:[9]
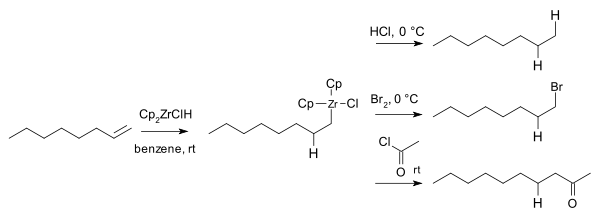
De overeenkomstige reacties met organoboor- en organoaluminiumverbindingen waren reeds bekend, maar de verbindingen zijn lucht-gevoelig en/of pyrofoor, terwijl organozirkoniumverbindingen dergelijke storende eigenschappen niet vertonen.
Toepassingen
Door toevoeging van zinkchloride kan de gebruikelijke regioselectiviteit van de alkyn-hydrozirkonering omgedraaid worden:[10][11]

Een voorbeeld van hydrozirkonering-carbonylering-koppeling is hieronder aangegeven:[12]

In reacties met een aantal allylalcoholen wordt de alcoholgroep vervangen door een nucleofiel koolstofatoom, waarbij een cyclopropaanring gevormd wordt:[13]

Navigatie Koolstof-elementbinding
Bronnen, noten en/of referenties
|






