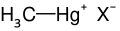Metylortęć
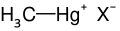 | X−
– dowolny anion | |
| Nazewnictwo | | | | Inne nazwy i oznaczenia | | kation monometylortęci(II) | |
| Ogólne informacje |
| Wzór sumaryczny | CH
3Hg+
|
| Masa molowa | 215,624 g/mol |
| Identyfikacja |
| Numer CAS | 22967-92-6 |
| PubChem | 6860 |
| |
| InChI | InChI=1S/CH3.Hg/h1H3;/q;+1 | | InChIKey | DBUXSCUEGJMZAE-UHFFFAOYSA-N | |
| Niebezpieczeństwa | Globalnie zharmonizowany system
klasyfikacji i oznakowania chemikaliów | | Na podstawie Rozporządzenia CLP, zał. VI[1] | | | | | | Zwroty H | H300, H310, H330, H373, H410 | | Zwroty P | brak wiarygodnych danych | |
 | Multimedia w Wikimedia Commons | |
 | Hasło w Wikisłowniku | |
Metylortęć – metaloorganiczny związek chemiczny z grupy związków rtęcioorganicznych, o bardzo wysokiej toksyczności oraz łatwości wnikania do organizmu. Metylortęć w środowisku pochodzi ze źródeł antropogenicznych (jako jeden z produktów ubocznych produkcji przemysłowej) i naturalnych (w wyniku procesu metylacji rtęci przeprowadzanego przez mikroorganizmy). W środowisku, szczególnie wodnym, ulega bioakumulacji i biomagnifikacji.
Metylortęć może być wchłaniana przez organizm zarówno drogą wziewną, pokarmową, jak i przez skórę. Wiąże się z białkami i wraz z krwią jest transportowana do tkanek i układów, głównie zaś do mózgu oraz nerek i wątroby. Może także przenikać przez łożysko i stanowić zagrożenie dla płodu, w którym się akumuluje. Jej toksyczność odbija się przede wszystkim na układzie nerwowym, powodując między innymi uszkodzenia komórek mózgowych. Powoduje ataksję, uszkodzenia słuchu i wzroku, zaburzenia psychiczne. Może też powodować uszkodzenia płodu. Metylortęć ma długi biologiczny okres półtrwania, co oznacza, że raz zgromadzona w organizmie pozostaje w nim przez długi czas, mogąc powodować choroby i uszkodzenia.
Ze względu na silne właściwości biobójcze metylortęć była stosowana w produkcji środków ochrony roślin (pestycydów). W Polsce, w czasach istnienia Państwowych Gospodarstw Rolnych stosowane były ogromne ilości tego środka[potrzebny przypis]. Obecnie produkcja i używanie pestycydów zawierających związki rtęci zostały prawnie zakazane jako zbyt zagrażające środowisku i zdrowiu ludzi[2].
Przypisy
- ↑ Organic compounds of mercury with the exception of those specified elsewhere in this Annex, [w:] Classification and Labelling Inventory, Europejska Agencja Chemikaliów (ang.).
- ↑ Rozporządzenie Komisji UE z dnia 16 stycznia 2018 r. zmieniające załączniki II i III do rozporządzenia (WE) nr 396/2005 Parlamentu Europejskiego i Rady w odniesieniu do najwyższych dopuszczalnych poziomów pozostałości związków rtęci w określonych produktach oraz na ich powierzchni. [dostęp 2018-10-27].
Bibliografia
- Friberg L., Nordberg G. F., Vou V. B. Handbook on the toxicology of metals. Wyd. 2. Elsevier Science Publishers B. V., Amsterdam, NY, Oxford, 1986.
Linki zewnętrzne
- Toksykologia żywieniowa i żywności
- Rtęć a spożycie ryb, „Allum – Alergia, Środowisko i Zdrowie”, 14 czerwca 2012 [dostęp 2017-01-28] [zarchiwizowane z adresu 2017-02-02] .
- ArturA. Kowalski ArturA. i inni, Rtęć w środowisku przyrodniczym [online], www.e-czytelnia.abrys.pl [dostęp 2017-01-28] .
- Rtęć, „Allum – Alergia, Środowisko i Zdrowie”, 13 czerwca 2012 [dostęp 2017-01-28] [zarchiwizowane z adresu 2017-02-02] .